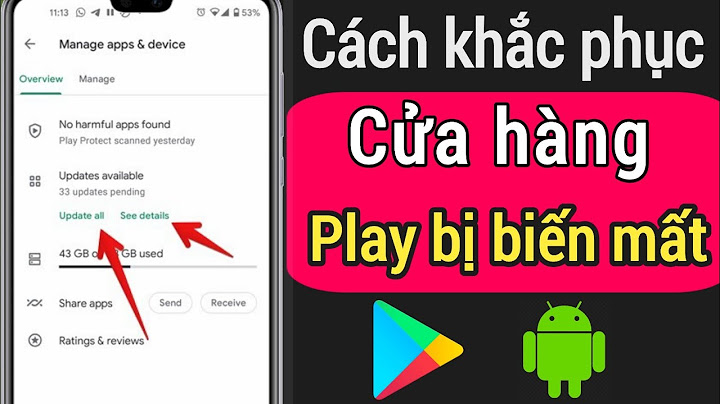
+ Đối với phản ứng cộng H 2 /Br 2 : nanken phản ứng=nH 2 = nBr 2+ Độ tăng khối lượng bình H 2 /Br 2 : m bình tăng=m anken phản ứng+ Độ giảm số mol khí sau phản ứng so với trước phản ứng: nanken phản ứng= nt -nsLưu ý: Sau khi cộng H 2 mà khối lượng mol trung bình của sản phẩm tạo thành nhỏ hơn 28 thì chắc chắn có H 2 dư B. Ví dụ minh họa Ví dụ 1: 2,8 gam anken X làm mất màu vừa đủ dung dịch chứa 8 gam Br 2. Hiđrat hóa X chỉ thu được một ancol duy nhất. X có tên là A. etilen. B. but-2-en. C. hex-2-en. D. 2,3-đimetylbut-2-en. Ví dụ 2: Hỗn hợp khí X gồm H 2 và C 2 H 4 có tỉ khối so với He là 3,75. Dẫn X qua Ni nung nóng, thu được hỗn hợp khí Y có tỉ khối so với He là 5. Tính hiệu suất của phản ứng hiđro hoá? A. 20% B. 25% C. 50% D. 40% Show Biết tỉ khối hơi của A đối với H 2 là 23,2. Hiệu suất phản ứng hiđro hoá là 75%. Công thức phân tử olefin A. C 2 H 4 B. C 3 H 6 C. C 4 H 8 D. C 5 H 10 Câu 8: Cho hiđrocacbon X phản ứng với brom (trong dung dịch) theo tỷ lệ mol 1: 1 thì được chất hữu cơ Y (chứa 74,08% brom về khối lượng). Khi X phản ứng với HBr thì thu được hai sản phẩm hữu cơ có cấu tạo khác nhau. Tên gọi của X là A. but-1-en B. etilen C. but-2-en D. propilen Câu 9: Trộn 1 mol anken X với 1,6 molH 2 rồi dẫn hỗn hợp qua Ni nung nóngthu được hỗn hợp Y. Dẫn hỗn hợp Y vàobrom dư thấy có 0,2 mol Br 2 đã phảnứng. Hiệu suất phản ứng hiđro hóa làA. 20%. B. 50%.C. 80%. D. 70%.Câu 10: Hỗn hợp X gồm H 2 , C 2 H 4 , C 3 H 6 có tỉ khối so với H 2 là 9,25. Cho 22,4 lit X (dktc) vào bình đựng kín có sẵn ít bột Ni. Đun nóng bình một thời gian thu được hỗn hợp khí Y có tỉ khối so với H 2 bằng 10. Tổng số mol H 2 đã phản ứng A. 0,070 mol B. 0,015 mol C. 0,075 mol D. 0,050 mol Dạng 2: Bài tập về phản ứng trùng hợp Anken và cách giải – Hóa học lớp 11 A. Lý thuyết và phương pháp giải Ở nhiệt độ cao, áp suất cao và xúc tác thích hợp, các phân tử anken có thể kết hợp với nhau tạo thành những phân tử có mạch rất dài và phân tử khối lớn. Ví dụ: Chú ý:
Lưu ý: Phản ứng làm mất màu tím của dung dịch KMnO 4 và tạo kết tủa đen MnO 2 dùng để phân biệt anken và ankan.
B. 50%C. 25%D. 75%Ví dụ 3: Để khử hoàn toàn 200 ml dung dịch KMnO 4 0,2M tạo thành chất rắn màu đen cần V lít khí C 2 H 4 (đktc). Giá trị tối thiểu của V là A. 0,224 (lít) B. 0,336 (lít) C. 0,672 (lít) D. 1,344 (lít) C. Bài tập tự luyện Câu 1: Đốt cháy hoàn toàn a gam hỗn hợp eten, propen, but-2-en cần dùng vừa đủ b lít oxi (ở đktc) thu được 2,4 mol CO 2. Giá trị của b là: A. 92,4 lít. B. 94,2 lít. C. 80,64 lít. D. 24,9 lít Câu 2: Anken A phản ứng hoàn toàn với dung dịch KMnO 4 được chất hữu cơ B có MB = 1,81MA. CTPT của A là: A. C 2 H 4 B. C 3 H 6 C. C 4 H 8 D. C 5 H 10 Câu 3: Đốt cháy hoàn toàn hỗn hợp gồm 0, mol C 2 H 4 và 0,2 mol C 3 H 6 thu được V lít khí CO 2 (đktc). Giá trị của V là A. 8,96. B. 17, C. 15,68. D. 13,44. Câu 4: Đốt cháy hoàn toàn m gam hỗn hợp X gồm các hiđrocacbon mạch hở: CH 4 , C 3 H 6 , C 4 H 8 thu được 4,4 gam CO 2 và 2,52 gam H 2 O. Phần trăm khối lượng CH 4 trong hỗn hợp X là A. 34,42%. B. 42,34%. C. 43,24%. D. 44,23%Câu 5: Cho 3,5g một anken tác dụng với dung dịch KMnO 4 loãng thì được 5,2g sản phẩm hữu cơ. CTPT của anken là A. C 3 H 6. B. C 4 H 8. C. C 5 H 10. D. C 6 H 12. Câu 6: Một hỗn hợp A gồm 2 hiđrocacbon X, Y liên tiếp nhau trong cùng dãy đồng đẳng (MX< MY). Đốt cháy 11,2 lít hỗn hợp A thu được 57,2 gam CO 2 và 23,4 gam H 2 O. CTPT X, Y và khối lượng của X, Y là: A. 12,6 gam C 3 H 6 và 11,2 gam C 4 H 8. B. 8,6 gam C 3 H 6 và 11,2 gam C 4 H 8. C. 5,6 gam C 2 H 4 và 12,6 gam C 3 H 6. D. 2,8 gam C 2 H 4 và 16,8 gam C 3 H 6. Câu 7: Đem đốt cháy hoàn toàn 0,1 mol hỗn hợp X gồm 2 anken là đồng đẳng kế tiếp nhau thu được CO 2 và nước có khối lượng hơn kém nhau 6,76 gam. CTPT của 2 anken đó là A. C 2 H 4 và C 3 H 6. B. C 3 H 6 và C 4 H 8. |