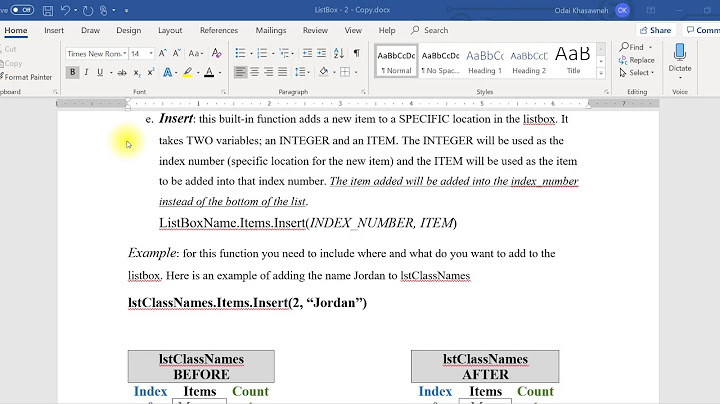
Hiđro có nguyên tử khối là 1,008. Hỏi có bao nhiêu nguyên tử của đồng vị \( _{1}{2}\textrm{H}\)trong 1ml nước (cho rằng trong nước chỉ có đồng vị \( _{1}{2}\textrm{H}\) và \( _{1}^{1}\textrm{H}\))? (Cho khối lượng riêng của nước là 1 g/ml). Video hướng dẫn giải Quảng cáo  Lời giải chi tiết Gọi % số nguyên tử đồng vị \( _{1}^{2}\textrm{H}\) là a%: \=> % của nguyên tử đồng vị \( _{1}^{1}\textrm{H}\) là (100-a)% \( \dfrac{1(100-a)+2a}{100}\) = 1,008 => a = 0,8 Vì D = 1 g/ml \=> Khối lượng của 1ml nước là 1 gam. \( Phân tử khối_{H_{2}O}\) = 16 + 1,008.2 = 18,016u \=> Khối lượng mol của nước là 18,016 g/mol Số mol của 1 gam nước là: \(\dfrac{1}{{18,016}} = 0,0555mol\) Số nguyên tử H có trong 1ml H2O: \(2.0,0555.6,{022.10^{23}} = 6,{68442.10^{22}}\) nguyên tử Số nguyên tử \( _{1}{2}\textrm{H}\) chiếm: \(6,{68442.10{22}}.\dfrac{{0,8}}{{100}} = 5,{35.10^{20}}\) nguyên tử Loigiaihay.com
Hãy xác định điện tích hạt nhân, số proton, số nơtron, số electron, nguyên tử khối của các nguyên tử thuộc các nguyên tố sau: Nguyên tố cacbon có hai đồng vị bền: \(_6^{12}C\) chiếm 98,89% và \(_6^{13}C\) chiếm 1,11%. Nguyên tử khối trung bình của nguyên tố cacbon là
Giải Ta có \({\overline M _C} = {{12.98,89 + 13.1,11} \over {100}} = 12,011\) (đvC) Chọn B. Bài 2 trang 14 SGK Hóa học 10 Nâng cao Cho biết số proton, số nơtron và số electron của các đồng vị sau đây:
Giải Kí hiệu nguyên tử Số proton Số nơtron Số electron \(\eqalign{ & a)\,\,\,\,\,_{14}{28}Si \cr & \,\,\,\,\,\,\,\,\,_{14}{29}Si \cr & \,\,\,\,\,\,\,\,\,_{14}^{30}Si \cr} \) \(\eqalign{ & 14 \cr & 14 \cr & 14 \cr} \) \(\eqalign{ & 14 \cr & 15 \cr & 16 \cr} \) \(\eqalign{ & 14 \cr & 14 \cr & 14 \cr} \) \(\eqalign{ & b)\,\,\,\,_{26}{54}Fe \cr & \,\,\,\,\,\,\,\,_{26}{56}Fe \cr & \,\,\,\,\,\,\,\,_{16}{57}Fe \cr & \,\,\,\,\,\,\,\,_{26}{58}Fe \cr} \) \(\eqalign{ & 26 \cr & 26 \cr & 26 \cr & 26 \cr} \) \(\eqalign{ & 28 \cr & 30 \cr & 31 \cr & 32 \cr} \) \(\eqalign{ & 26 \cr & 26 \cr & 26 \cr & 26 \cr} \) Bài 3 trang 14 SGK Hóa học 10 Nâng cao Nguyên tử khối trung bình của bạc bằng 107,02 lần nguyên tử khối của hiđro. Nguyên tử khối của hiđro bằng 1,008. Tính nguyên tử khối trung bình của bạc. Giải Theo đề bài ta có \({\overline A _{Ag}} = 107,02.{M_H} = 107,02.1,008 = 107,876u.\) Bài 4 trang 14 SGK Hóa học 10 Nâng cao Cho hai đồng vị hiđro và hai đồng vị clo với tỉ lệ phần trăm số nguyên tử chiếm trong tự nhiên như sau: \(_1^1H\,\,\left( {99,984\% } \right),\,\,_1^2H\,\,\left( {0,016\% } \right)\) \(_{17}{35}Cl\,\,\left( {75,77\% } \right),\,\,_{17}{37}Cl\,\,\left( {24,23\% } \right).\)
Giải
Áp dụng công thức: \(\overline A = {{aA + bB} \over {a + b}}\) Ta tính được \({\overline A _H} = 1,00016u,{\overline A _{Cl}} = 35,4846u.\)
Công thức phân tử: \(H_{17}{35}Cl;\,\,H_{17}{37}Cl;\,\,D_{17}{35}Cl;\,\,D_{17}{37}Cl.\)
Bài 5 trang 14 SGK Hóa học 10 Nâng cao Nguyên tử khối trung bình của đồng bằng 63,546. Trong tự nhiên, đồng có hai đồng vị \(_{29}{63}Cu\) và \(_{29}{65}Cu\). Tính tỉ lệ phần trăm số nguyên tử của đồng vị \(_{29}^{63}Cu\) tồn tại trong tự nhiên. Giải Gọi x là phần trăm của đồng vị \(_{29}{63}Cu \Rightarrow \) phần trăm của đồng vị \(_{29}{65}Cu\) là (100 – x). Ta có: \({\overline A _{Cu}} = {{63.x + 65\left( {100 - x} \right)} \over {100}} = 63,546 \Rightarrow x \approx 73.\) Vậy tỉ lệ phần trăm số nguyên tử của đồng vị \(_{29}^{63}Cu\) là 73%. Bài 6 trang 14 SGK Hóa học 10 Nâng cao Cho hai đồng vị \(_1^1H\) (kí hiệu là H) và \(_1^2H\) (kí hiệu là D).
|